Большая Советская Энциклопедия (СЖ)
Сжатие
Сжа'тие в сопротивлении материале в, см.
Растяжение-сжатие.
(обратно)
Сжатие земли
Сжа'тие земли', земного эллипсоида, величина, характеризующая степень сплюснутости Земли в направлении оси вращения, т. е. отступление формы Земли от шара. Полярное С. З. a выражается равенством:

, где
a — радиус экватора Земли, а
b — полярный радиус её. По современным данным, a = 1: 298,3. В связи с обнаруженным фактом сплюснутости Земли также и по экватору введено понятие экваториального С. З., равного

, где
a1 и
a2, соответственно, — наибольший и наименьший радиусы земного экватора. По имеющимся данным, e = 1: 30000, разность
a1 — a2 составляет около 210
м. См. также
Геодезия,
Земля.
(обратно)
Сжатых отображений принцип
Сжа'тых отображе'ний при'нцип, одно из основных положений теории
метрических пространств о существовании и единственности неподвижной точки множества при некотором специальном («сжимающем») отображении его в себя. С. о. п. применяют главным образом в теории дифференциальных и интегральных уравнений. Произвольное отображение
А метрического пространства
М в себя, которое каждой точке
х из
М сопоставляет некоторую точку
у = Ax из
М, порождает в пространстве
М уравнение
Ax = х. (*) Действие отображения
А на точку
х можно интерпретировать как перемещение её в точку
у = Ax. Точка
х называется неподвижной точкой отображения
А, если выполняется равенство (*). Т. о. вопрос о разрешимости уравнения (*) является вопросом о нахождении неподвижных точек отображения
А.
Отображение
А метрического пространства
М в себя называется сжатым, если существует такое положительное число a < 1, что для любых точек
х и
у из
М выполняется неравенство
d (
Ax, Ау) £ a
d (
х, у),
где символ
d (
u, u) означает расстояние между точками
u и u метрического пространства
М.
С. о. п. утверждает, что каждое сжатое отображение полного метрического пространства в себя имеет, и притом только одну, неподвижную точку. Кроме того, для любой начальной точки
x0 из
М последовательность {
xn}, определяемая рекуррентными соотношениями
xn = Axn-1,
n = 1,2,..., имеет своим пределом неподвижную точку
х отображения
А. При этом справедлива следующая оценка погрешности:

. С. о. п. позволяет единым методом доказывать важные теоремы о существовании и единственности решений дифференциальных, интегральных и др. уравнений. В условиях применимости С. о. п. решение может быть с наперёд заданной точностью вычислено
последовательных приближений методом.
С помощью определённого выбора полного метрического пространства
М и построения отображения
А эти задачи сводят предварительно к уравнению (*), а затем находят условия, при которых отображение
А оказывается сжатым.
Лит.: Смирнов В. И., Курс высшей математики, т. 5, М., 1959.
Ш. А. Алимов.
(обратно)
Сжижение газов
Сжиже'ние га'зов, переход вещества из газообразного состояния в жидкое. С. г. достигается охлаждением их ниже
критической температуры (
Тк) и последующей конденсацией в результате отвода теплоты парообразования (конденсации). Охлаждение газа ниже
ТК необходимо для достижения области температур, при которых газ может сконденсироваться в жидкость (при
Т >
ТК жидкость существовать не может). Впервые газ (аммиак) был сжижен в 1792 (голландский физик М. ван Марум). Хлор был получен в жидком состоянии в 1823 (М.
Фарадей), кислород — в 1877 (швейцарский учёный Р. Пикте и французский учёный Л. П. Кальете), азот и окись углерода — в 1883 (З. Ф.
Вроблевский и К.
Ольшевский), водород — в 1898 (Дж.
Дьюар), гелий — в 1908 (Х.
Камерлинг-Оннес). Идеальный процесс С. г. изображен на
рис. 1. Изобара
1—2 соответствует охлаждению газа до начала конденсации, изотерма
2—0 — конденсации газа. Площадь ниже
1—2—0 эквивалентна количеству теплоты, которое необходимо отвести от газа при его сжижении, а площадь внутри контура
1—2—0—3 (
1—3 — изотермическое сжатие газа,
3—0 — адиабатическое его расширение) характеризует термодинамически минимальную работу
Lmin, необходимую для С. г.:
Lmin =
T0(
SГ — SЖ)
— (
JГ - JЖ), где
T0 — температура окружающей среды;
SГ,
SЖ — энтропии газа и жидкости;
JГ,
JЖ — теплосодержания (энтальпии) газа и жидкости. Значения
Lmin и действительно затрачиваемой работы
LД для сжижения ряда газов даны в таблице. Промышленное С. г. с критической температурой
ТК выше температуры окружающей среды (например, аммиак, хлор) осуществляется с помощью компрессора, где газ сжимается, и последующей конденсацией газа в теплообменниках, охлаждаемых водой или холодильным рассолом. С. г. с
ТК, которая значительно ниже температуры окружающей среды, производится методами
глубокого охлаждения. Наиболее часто для С. г. с низким
ТК применяются
холодильные циклы, основанные на дросселировании сжатого газа (использование
Джоуля — Томсона эффекта), на расширении сжатого газа с производством внешней работы в детандере, на расширении газа из постоянного объёма без совершения внешней работы (метод
теплового насоса). В лабораторной практике иногда используется
каскадный метод охлаждения (сжижения). Графическое изображение и схема дроссельного цикла С. г. дана на
рис. 2. После сжатия в компрессоре (
1—2) газ последовательно охлаждается в теплообменниках (
2—3—4) и затем расширяется (дросселируется) в вентиле (
4—5). При этом часть газа сжижается и скапливается в сборнике, а несжижившийся газ направляется в теплообменники и охлаждает свежие порции сжатого газа. Для С. г. по циклу с дросселированием необходимо, чтобы температура сжатого газа перед входом в основной теплообменник T3 была ниже температуры инверсионной точки (см.
Инверсионная кривая). Для этого и служит теплообменник с посторонним
холодильным агентом T2. Если температура инверсионной точки газа лежит выше комнатной (азот, аргон, кислород), то схема принципиально работоспособна и без теплообменников T1 и T2. Применение посторонних хладагентов в этих случаях имеет целью повышение выхода жидкости. Если же температура инверсионной точки газа ниже комнатной, то теплообменник с посторонним хладагентом обязателен. Например, при сжижении водорода методом дросселирования в качестве постороннего хладагента используется жидкий азот, при сжижении гелия — жидкий водород. Для С. г. в промышленных масштабах чаще всего применяются циклы с детандерами (
рис. 3), т. к. расширение газов с производством внешней работы — наиболее эффективный метод охлаждения. В самом детандере жидкость обычно не получают, ибо технически проще проводить само сжижение в дополнительной дроссельной ступени. После сжатия в компрессоре (
1—2) и предварительного охлаждения в теплообменнике (
2—3) поток сжатого газа делится на 2 части: часть
М отводится в детандер, где, расширяясь, производит внешнюю работу и охлаждается (
3—7). Охлажденный газ подаётся в теплообменник, где понижает температуру оставшейся части сжатого газа
1 — М, которая затем дросселируется и сжижается. Теоретически расширение в детандере должно осуществляться при постоянной энтропии (
3—6). Однако из-за потерь расширение протекает по линии
3—7. Для увеличения термодинамической эффективности процесса С. г. иногда применяют несколько детандеров, работающих на различных температурных уровнях. Циклы с тепловыми насосами обычно используются (наряду с детандерными и дроссельными циклами) при С. г. с помощью холодильно-газовых машин, которые позволяют получать температуры до 12 К, что достаточно для сжижения всех газов, кроме гелия (см. табл.). Для сжижения гелия к машине пристраивается дополнительная дроссельная ступень. Подвергаемые сжижению газы должны очищаться от паров воды, масла и др. примесей (например, воздух — от углекислоты, водород — от воздуха), которые при охлаждении могут затвердеть и закупорить теплообменную аппаратуру. Поэтому узел очистки газа от посторонних примесей — необходимая часть установок С. г. О применении сжиженных газов см. в ст.
Глубокое охлаждение. Значения температуры кипения
Ткип (при 760
мм. рт. ст.), критической температуры
ТК, минимальной
Lmin и действительной
LД работ сжижения некоторых газов
| Газ | Ткип, К | ТК, К | Lmin, квт•ч/кг | Lд, квт•ч/кг |
| Азот Аргон Водород Воздух Гелий Кислород Метан Неон Пропан Этилен | 77,4 87,3 20,4 78,8 4,2 90,2 111,7 27,1 231,1 169,4 | 126,2 150,7 33,0 132,5 5,3 154,2 191,1 44,5 370,0 282,6 | 0,220 0,134 3,31 0,205 1,93 0,177 0,307 0,37 0,04 0,119 | 1,2—1,5 0,8—0,95 15—40 1,25—1,5 15—25 1,2—1,4 0,75—1,2 3—4 ~ 0,08 ~ 0,3 |
Лит.: Фастовский В. Г., Петровский Ю. В., Ровинский А. Е., Криогенная техника, 2 изд., М., 1974; Справочник по физико-техническим основам криогеники, 2 изд., М., 1973. См. также лит. при ст.
Глубокое охлаждение.
А. Б. Фрадков. 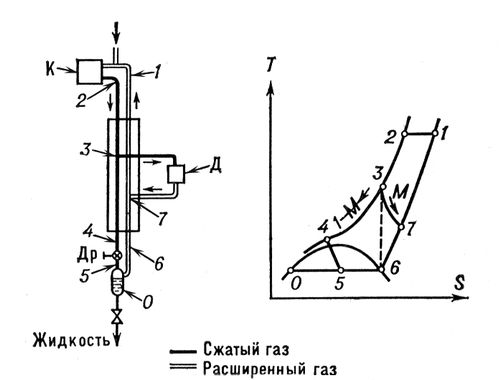
Рис. 3. Схема и диаграмма Т — S (температура — энтропия) цикла сжижения газов с детандером: К — компрессор; Д — детандер; Др — дроссельный вентиль.

Рис. 1. Идеальный цикл сжижения газов на диаграмме T—S (температура — энтропия).

Рис. 2. Схема и диаграмма Т — S (температура — энтропия) цикла сжижения газов на основе эффекта Джоуля — Томсона: К — компрессор; T1, T2, ТЗ — теплообменники; Др — дроссельный вентиль.
(обратно)
Сжимаемость
Сжима'емость, способность вещества изменять свой объём под действием всестороннего давления. С. обладают все вещества. Если вещество в процессе сжатия не испытывает химических, структурных и других изменений, то при возвращении внешнего давления к исходному значению начальный объём восстанавливается. У твёрдых тел, имеющих поры, трещины и другие неоднородности структуры, практически обратимая С. может наблюдаться только при достаточно высоком давлении (например, у горных пород при давлении большем 2—5
кбар; 1
кбар = 10
8 н/м2).
Обычно С. (объёмной упругостью) называется обратимое изменение занимаемого веществом объёма
V под равномерным гидростатическим давлением
р. Величину С. характеризует коэффициент С. (b, который выражает уменьшение единичного объёма тела при увеличении
р на одну единицу:

, где D
V и Dr — изменения объёма
V и плотности r при изменении
р на величину D
р.
К = 1/b называют модулем объёмной упругости (модулем объёмного сжатия, объёмным модулем), для твердых тел

, где
Е — модуль нормальной упругости (
Юнга модуль), m — модуль сдвига. Для идеальных газов
К = р при любой температуре
Т. В общем случае С. вещества, а следовательно
К и b, зависит от
р и
Т. Как правило, b убывает при увеличении
р и растет с
Т. Часто С. характеризуют относит. плотностью d = r/r
0, где r
0 — плотность при О °С и
р = 1
атм.
Сжатие может происходить как при постоянной температуре (изотермически), так и с одновременным разогревом сжимаемого тела (например, в адиабатном процессе). В последнем случае значения
К будут большими, чем при изотермическом сжатии (для большинства твёрдых тел при обычной температуре — на несколько %). Для оценки С. веществ в широком диапазоне давлений используют уравнения состояния, выражающие связь между
р,
V и
Т. Определяют С. непосредственно по изменению объёма тел под давлением (см.
Пьезометр), из акустических измерений скорости распространения упругих волн в веществе, из экспериментов по ударному сжатию, дающих зависимость между r и
р при максимальных полученных в эксперименте давлениях. С. находят также из измерений параметров кристаллической решётки под давлением, производимых методом
рентгеновского структурного анализа. С. можно определить с помощью измерения линейной деформации твёрдого тела под гидростатическим давлением (по т. н. линейной С.). Для изотропного тела коэффициент линейной С.

, где
L — линейный размер тела. С. газов, будучи очень большой при давлениях до 1
кбар, по мере приближения их плотности к плотности жидкостей становится близкой к С. жидкостей. Последняя с ростом
р уменьшается сначала резко, а затем меняется весьма мало: в интервале 6—12
кбар b уменьшается примерно так же, как в интервале от 1
атм (10
-3 кбар) до 1
кбар (примерно в 2 раза), и при 10—12
кбар составляет 5—10% от начального значения. При 30—50
кбар модули
К жидкостей по порядку величины близки к
К твёрдых тел. Для твёрдых тел при 100
кбар Dr/r
0 » 15—25%. Для отдельных веществ, например щелочных металлов, Dr/r ~ 40%, для большинства др. металлов ~ 6—15%. Линейная С. анизотропных веществ зависит от кристаллографических направлений (во всяком случае, до давлений в десятки
кбар), причём вдоль направлений со слабым межатомным взаимодействием она может в 8—10 раз превосходить С. по направлениям, вдоль которых в кристаллической решётке имеет место более сильная связь; изменение параметра решётки в этих направлениях в определённом интервале
р может быть даже положительным (теллур, селен). С. — важнейшая характеристика вещества, которая позволяет судить о зависимости физических свойств от межатомных (межмолекулярных) расстояний. Знание С. газов (паров), жидкостей и твёрдых тел необходимо для расчёта работы тепловых машин, химико-технологических процессов, действия взрыва, аэро- и гидродинамических эффектов, наблюдающихся при движениях с большими скоростями, и т. д. Примеры С. различных веществ приведены в ст.
Давление высокое.
Лит.: Варгафтик Н. Б., Справочник по теплофизическим свойствам газов и жидкостей, 2 изд., М., 1972; Справочник физических констант горных пород, [пер. с англ.], М., 1969, гл. 7; Физический энциклопедический словарь, т. 4, М., 1963 (ст. Сжимаемость). См. также лит. при статьях
Давление высокое.
Пьезометр.
Л. Д. Лившиц.
(обратно)
Оглавление
СжатиеСжатие землиСжатых отображений принципСжижение газовСжимаемость
 , где a — радиус экватора Земли, а b — полярный радиус её. По современным данным, a = 1: 298,3. В связи с обнаруженным фактом сплюснутости Земли также и по экватору введено понятие экваториального С. З., равного
, где a — радиус экватора Земли, а b — полярный радиус её. По современным данным, a = 1: 298,3. В связи с обнаруженным фактом сплюснутости Земли также и по экватору введено понятие экваториального С. З., равного  , где a1 и a2, соответственно, — наибольший и наименьший радиусы земного экватора. По имеющимся данным, e = 1: 30000, разность a1 — a2 составляет около 210 м. См. также Геодезия, Земля.
(обратно)
, где a1 и a2, соответственно, — наибольший и наименьший радиусы земного экватора. По имеющимся данным, e = 1: 30000, разность a1 — a2 составляет около 210 м. См. также Геодезия, Земля.
(обратно)
 . С. о. п. позволяет единым методом доказывать важные теоремы о существовании и единственности решений дифференциальных, интегральных и др. уравнений. В условиях применимости С. о. п. решение может быть с наперёд заданной точностью вычислено последовательных приближений методом. С помощью определённого выбора полного метрического пространства М и построения отображения А эти задачи сводят предварительно к уравнению (*), а затем находят условия, при которых отображение А оказывается сжатым. Лит.: Смирнов В. И., Курс высшей математики, т. 5, М., 1959. Ш. А. Алимов.
(обратно)
. С. о. п. позволяет единым методом доказывать важные теоремы о существовании и единственности решений дифференциальных, интегральных и др. уравнений. В условиях применимости С. о. п. решение может быть с наперёд заданной точностью вычислено последовательных приближений методом. С помощью определённого выбора полного метрического пространства М и построения отображения А эти задачи сводят предварительно к уравнению (*), а затем находят условия, при которых отображение А оказывается сжатым. Лит.: Смирнов В. И., Курс высшей математики, т. 5, М., 1959. Ш. А. Алимов.
(обратно)
 Рис. 3. Схема и диаграмма Т — S (температура — энтропия) цикла сжижения газов с детандером: К — компрессор; Д — детандер; Др — дроссельный вентиль.
Рис. 3. Схема и диаграмма Т — S (температура — энтропия) цикла сжижения газов с детандером: К — компрессор; Д — детандер; Др — дроссельный вентиль. Рис. 1. Идеальный цикл сжижения газов на диаграмме T—S (температура — энтропия).
Рис. 1. Идеальный цикл сжижения газов на диаграмме T—S (температура — энтропия). Рис. 2. Схема и диаграмма Т — S (температура — энтропия) цикла сжижения газов на основе эффекта Джоуля — Томсона: К — компрессор; T1, T2, ТЗ — теплообменники; Др — дроссельный вентиль.
(обратно)
Рис. 2. Схема и диаграмма Т — S (температура — энтропия) цикла сжижения газов на основе эффекта Джоуля — Томсона: К — компрессор; T1, T2, ТЗ — теплообменники; Др — дроссельный вентиль.
(обратно)
 , где DV и Dr — изменения объёма V и плотности r при изменении р на величину Dр. К = 1/b называют модулем объёмной упругости (модулем объёмного сжатия, объёмным модулем), для твердых тел
, где DV и Dr — изменения объёма V и плотности r при изменении р на величину Dр. К = 1/b называют модулем объёмной упругости (модулем объёмного сжатия, объёмным модулем), для твердых тел  , где Е — модуль нормальной упругости (Юнга модуль), m — модуль сдвига. Для идеальных газов К = р при любой температуре Т. В общем случае С. вещества, а следовательно К и b, зависит от р и Т. Как правило, b убывает при увеличении р и растет с Т. Часто С. характеризуют относит. плотностью d = r/r0, где r0 — плотность при О °С и р = 1 атм. Сжатие может происходить как при постоянной температуре (изотермически), так и с одновременным разогревом сжимаемого тела (например, в адиабатном процессе). В последнем случае значения К будут большими, чем при изотермическом сжатии (для большинства твёрдых тел при обычной температуре — на несколько %). Для оценки С. веществ в широком диапазоне давлений используют уравнения состояния, выражающие связь между р, V и Т. Определяют С. непосредственно по изменению объёма тел под давлением (см. Пьезометр), из акустических измерений скорости распространения упругих волн в веществе, из экспериментов по ударному сжатию, дающих зависимость между r и р при максимальных полученных в эксперименте давлениях. С. находят также из измерений параметров кристаллической решётки под давлением, производимых методом рентгеновского структурного анализа. С. можно определить с помощью измерения линейной деформации твёрдого тела под гидростатическим давлением (по т. н. линейной С.). Для изотропного тела коэффициент линейной С.
, где Е — модуль нормальной упругости (Юнга модуль), m — модуль сдвига. Для идеальных газов К = р при любой температуре Т. В общем случае С. вещества, а следовательно К и b, зависит от р и Т. Как правило, b убывает при увеличении р и растет с Т. Часто С. характеризуют относит. плотностью d = r/r0, где r0 — плотность при О °С и р = 1 атм. Сжатие может происходить как при постоянной температуре (изотермически), так и с одновременным разогревом сжимаемого тела (например, в адиабатном процессе). В последнем случае значения К будут большими, чем при изотермическом сжатии (для большинства твёрдых тел при обычной температуре — на несколько %). Для оценки С. веществ в широком диапазоне давлений используют уравнения состояния, выражающие связь между р, V и Т. Определяют С. непосредственно по изменению объёма тел под давлением (см. Пьезометр), из акустических измерений скорости распространения упругих волн в веществе, из экспериментов по ударному сжатию, дающих зависимость между r и р при максимальных полученных в эксперименте давлениях. С. находят также из измерений параметров кристаллической решётки под давлением, производимых методом рентгеновского структурного анализа. С. можно определить с помощью измерения линейной деформации твёрдого тела под гидростатическим давлением (по т. н. линейной С.). Для изотропного тела коэффициент линейной С.  , где L — линейный размер тела. С. газов, будучи очень большой при давлениях до 1 кбар, по мере приближения их плотности к плотности жидкостей становится близкой к С. жидкостей. Последняя с ростом р уменьшается сначала резко, а затем меняется весьма мало: в интервале 6—12 кбар b уменьшается примерно так же, как в интервале от 1 атм (10-3 кбар) до 1 кбар (примерно в 2 раза), и при 10—12 кбар составляет 5—10% от начального значения. При 30—50 кбар модули К жидкостей по порядку величины близки к К твёрдых тел. Для твёрдых тел при 100 кбар Dr/r0 » 15—25%. Для отдельных веществ, например щелочных металлов, Dr/r ~ 40%, для большинства др. металлов ~ 6—15%. Линейная С. анизотропных веществ зависит от кристаллографических направлений (во всяком случае, до давлений в десятки кбар), причём вдоль направлений со слабым межатомным взаимодействием она может в 8—10 раз превосходить С. по направлениям, вдоль которых в кристаллической решётке имеет место более сильная связь; изменение параметра решётки в этих направлениях в определённом интервале р может быть даже положительным (теллур, селен). С. — важнейшая характеристика вещества, которая позволяет судить о зависимости физических свойств от межатомных (межмолекулярных) расстояний. Знание С. газов (паров), жидкостей и твёрдых тел необходимо для расчёта работы тепловых машин, химико-технологических процессов, действия взрыва, аэро- и гидродинамических эффектов, наблюдающихся при движениях с большими скоростями, и т. д. Примеры С. различных веществ приведены в ст. Давление высокое. Лит.: Варгафтик Н. Б., Справочник по теплофизическим свойствам газов и жидкостей, 2 изд., М., 1972; Справочник физических констант горных пород, [пер. с англ.], М., 1969, гл. 7; Физический энциклопедический словарь, т. 4, М., 1963 (ст. Сжимаемость). См. также лит. при статьях Давление высокое. Пьезометр. Л. Д. Лившиц.
(обратно)
, где L — линейный размер тела. С. газов, будучи очень большой при давлениях до 1 кбар, по мере приближения их плотности к плотности жидкостей становится близкой к С. жидкостей. Последняя с ростом р уменьшается сначала резко, а затем меняется весьма мало: в интервале 6—12 кбар b уменьшается примерно так же, как в интервале от 1 атм (10-3 кбар) до 1 кбар (примерно в 2 раза), и при 10—12 кбар составляет 5—10% от начального значения. При 30—50 кбар модули К жидкостей по порядку величины близки к К твёрдых тел. Для твёрдых тел при 100 кбар Dr/r0 » 15—25%. Для отдельных веществ, например щелочных металлов, Dr/r ~ 40%, для большинства др. металлов ~ 6—15%. Линейная С. анизотропных веществ зависит от кристаллографических направлений (во всяком случае, до давлений в десятки кбар), причём вдоль направлений со слабым межатомным взаимодействием она может в 8—10 раз превосходить С. по направлениям, вдоль которых в кристаллической решётке имеет место более сильная связь; изменение параметра решётки в этих направлениях в определённом интервале р может быть даже положительным (теллур, селен). С. — важнейшая характеристика вещества, которая позволяет судить о зависимости физических свойств от межатомных (межмолекулярных) расстояний. Знание С. газов (паров), жидкостей и твёрдых тел необходимо для расчёта работы тепловых машин, химико-технологических процессов, действия взрыва, аэро- и гидродинамических эффектов, наблюдающихся при движениях с большими скоростями, и т. д. Примеры С. различных веществ приведены в ст. Давление высокое. Лит.: Варгафтик Н. Б., Справочник по теплофизическим свойствам газов и жидкостей, 2 изд., М., 1972; Справочник физических констант горных пород, [пер. с англ.], М., 1969, гл. 7; Физический энциклопедический словарь, т. 4, М., 1963 (ст. Сжимаемость). См. также лит. при статьях Давление высокое. Пьезометр. Л. Д. Лившиц.
(обратно)